摘要:以一個無菌制劑車間的改造為例,對新版藥品GMP中無菌藥品附錄的生產(chǎn)要求進行討論,從工藝設(shè)計的角度分析,使改造設(shè)計滿足新規(guī)范要求。
關(guān)鍵詞:新版藥品GMP;無菌制劑車間;設(shè)計
《藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂)》已于2010年10月19日經(jīng)衛(wèi)生部部務(wù)會議審議通過,并與2011年3月1日起施行。本次修訂涉及基本要求以及無菌藥品、中藥制劑、原料藥、生物制品和血液制品五個附錄,其中無菌藥品是本次規(guī)范修訂的一個重點,變化也最大。隨著新版藥品GMP的施行,大批無菌藥品生產(chǎn)車間面臨改造,如何使我們的設(shè)計符合新規(guī)范的要求,從硬件上保證無菌藥品生產(chǎn)的安全及工藝流暢,對于設(shè)計人員是一個新的課題。本文以實際設(shè)計中的一個無菌制藥車間的改造為例,在工藝方面對新版藥品GMP的無菌藥品生產(chǎn)要求進行分析和探討。
1、新版藥品GMP無菌藥品生產(chǎn)相關(guān)要點
無菌藥品是指法定藥品標準中列有無菌檢查項目的制劑和原料包,包括無菌制劑和無菌原料藥,根據(jù)生產(chǎn)工藝又可分為最終滅菌產(chǎn)品及非最終滅菌產(chǎn)品兩類。為保證無菌藥品的安全和質(zhì)量提供法規(guī)和科學(xué)依據(jù),新版規(guī)范采用了歐盟和WHO的A、B、C、D分級標準,對無菌藥品生產(chǎn)的潔凈度級別提出了非常具體的要求懸浮粒子的靜態(tài)、動態(tài)監(jiān)測、浮游菌、沉降菌和表面微生物的監(jiān)測,細化了培養(yǎng)基模擬灌裝、滅菌驗證和管理的要求,增加了無菌操作的具體要求,強化了無菌保證的措施。
較原98版GMP標準,無菌藥品生產(chǎn)環(huán)境的潔凈度要求提高了。在潔凈區(qū)分級上,原有的100級、1萬級(包括無菌1萬級)、10萬級、30萬級等,均改為與歐盟標準相當(dāng)?shù)腁、B、C、D級。
A級是指高風(fēng)險操作區(qū),如灌裝區(qū)、放置膠塞桶和與無菌制劑直接接觸的敞口包裝容器的區(qū)域及無菌裝配或鏈接操作的區(qū)域,應(yīng)當(dāng)用單向流操作臺(罩)維持該區(qū)的環(huán)境狀態(tài)。B級指無菌配制和灌裝等高風(fēng)險操作A級潔凈區(qū)所處的背景區(qū)域。C級和D級指無菌藥品生產(chǎn)過程中重要程度較低操作步驟的潔凈區(qū)。潔凈區(qū)的潔凈度要求分“靜態(tài)”和“動態(tài)”標準,同時對潔凈區(qū)的懸浮粒子和微生物進行動態(tài)監(jiān)測。各級別空氣懸浮粒子的標準規(guī)定如表1
表1 各級潔凈度空氣懸浮粒子標準
| 潔凈度級別 | 懸浮粒子最大允許數(shù)/ m³ | |||
| 靜態(tài) | 動態(tài) | |||
| ≥0.5μm | ≥5.0μm | ≥0.5μm | ≥5.0μm | |
| A級 | 3520 | 20 | 3520 | 20 |
| B級 | 3520 | 29 | 352000 | 2900 |
| C級 | 352000 | 2900 | 3520000 | 29000 |
| D級 | 3520000 | 29000 | 不作規(guī)定 | 不作規(guī)定 |
2、無菌制劑車間改造實例
廣東某制藥有限公司一無菌制劑車間,生產(chǎn)非最終滅菌產(chǎn)品,現(xiàn)須根據(jù)新版GMP的要求,對原車間進行原地的改造設(shè)計。原車間的設(shè)備平面布置圖間圖1。
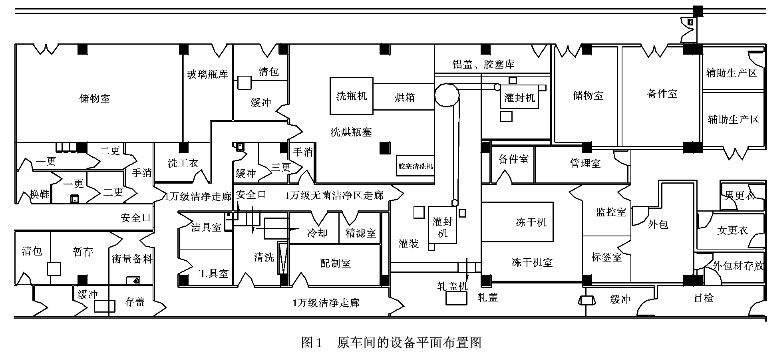
對非最終滅菌的產(chǎn)品,由于產(chǎn)品裝入最終容器后,不再作進一步的滅菌處理,因此必須對整個無菌藥品的生產(chǎn)過程及其環(huán)境條件進行嚴格的控制,以保證整個生產(chǎn)過程不被微生物所污染。具體操作分級見表2。
表2操作分級表
| 潔凈度級別 | 非最終滅菌產(chǎn)品的無菌生產(chǎn)操作示例 |
| B級背景下的A級 |
1.處于未完全密封狀態(tài)下產(chǎn)品的操作和轉(zhuǎn)運,如產(chǎn)品灌裝(或灌封)、分裝、壓塞、軋蓋等; 2.灌裝前無法除菌過濾的藥液或產(chǎn)品的配制; 3.直接接觸藥品的包裝材料、器皿滅菌后的裝配以及處于未完全密封狀態(tài)下的轉(zhuǎn)運和存放; 4.無菌原料藥的粉碎、過篩、混合、分裝。 |
| B級 |
1.處于未完全密封(1)狀態(tài)下的產(chǎn)品置于完全密封容器內(nèi)的轉(zhuǎn)運; 2.直接接觸藥品的包裝材料、器皿滅菌后處于密閉容器內(nèi)的轉(zhuǎn)運和存放。 |
| C級 |
1.灌裝前可除菌過濾的藥液或產(chǎn)品的配制; 2.產(chǎn)品的過濾 |
| D級 | 直接接觸藥品的包裝材料、器具的最終清洗、裝配或包裝、滅菌。 |
其中軋蓋前產(chǎn)品視為處于未完全密封狀態(tài)。根據(jù)已壓塞產(chǎn)品的密封性、軋蓋設(shè)備的設(shè)計、鋁蓋的特性等因素,軋蓋操作可選擇在C級或D級背景下的A級送風(fēng)環(huán)境中進行。A級送風(fēng)環(huán)境應(yīng)當(dāng)至少符合A級區(qū)的靜態(tài)要求。
2.2原車間改造要點
原車間在工藝布局上有幾個不足之處,也不能滿足新版規(guī)范要求,以下作分析討論。
(1)洗瓶滅菌區(qū)不應(yīng)與配液在同一級別區(qū)域進行生產(chǎn),灌裝前可除菌過濾的藥液或產(chǎn)品的配制工序,相對洗瓶滅菌的生產(chǎn)過程及其環(huán)境條件要嚴格,潔凈度要求也相應(yīng)要高,如果在同一區(qū)域生產(chǎn),生產(chǎn)人員穿插于2個不同要求的工序,共用同一人員凈化通道,生產(chǎn)中使用的容器具共用同一清潔間清洗,容易對配液工序產(chǎn)生影響,在工藝和空調(diào)上會容易造成污染。按照新GMP要求,配液須設(shè)置在C級;洗瓶滅菌應(yīng)該設(shè)置在D級區(qū)。
(2)無菌生產(chǎn)核心區(qū)需要考慮A級保護,包括了無菌藥品的灌裝區(qū)、滅菌后的瓶、塞、蓋進入無菌操作的區(qū)域、灌裝后半加塞產(chǎn)品等待凍干及凍干后產(chǎn)品暫存區(qū)域、無菌過濾器的連接組裝區(qū)域等;進入無菌區(qū)的工器具清洗后等待滅菌區(qū),以及滅菌后的存放區(qū)域,如果沒有采取其他密封保護措施,直接暴露的,也需加設(shè)A級送風(fēng)保護。
(3)由于軋蓋前產(chǎn)品視為處于未完全密封狀態(tài),因此操作需要在A級的環(huán)境保護下進行,軋蓋區(qū)同樣屬于無菌生產(chǎn)核心區(qū)。但是由于軋蓋會產(chǎn)生大量非活性的微粒,會隨著氣流飛揚,粘在設(shè)備和操作人員人體表面,在生產(chǎn)環(huán)境保護的同時也是一個污染源,若與灌裝操作區(qū)放在同一區(qū)域,使用同一B級區(qū)的空調(diào)系統(tǒng),則會造成產(chǎn)品和生產(chǎn)環(huán)境的污染。因此在布局上,考慮軋蓋操作區(qū)獨立設(shè)置,人員單獨更衣,在氣流組織上,軋蓋區(qū)相對灌裝區(qū)負壓;考慮到該工序的特殊性,可設(shè)置為C級背景下的A級送風(fēng)保護下進行操作。
綜合以上幾點,該無菌產(chǎn)品的生產(chǎn)流程及潔凈分區(qū)示意圖見圖2。
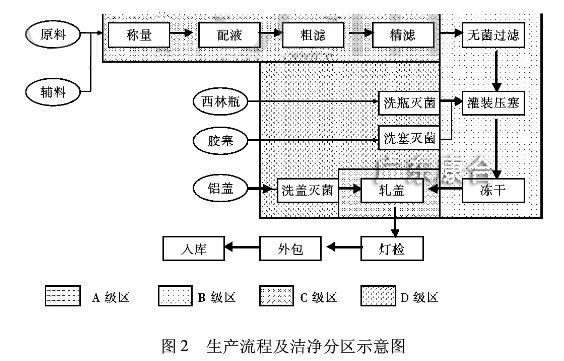
(5)加設(shè)B、C、D級各區(qū)廢品通道,B級區(qū)廢棄物由緩沖室傳遞柜傳出;考慮到生產(chǎn)中人工操作需使用到哦周轉(zhuǎn)盤,加設(shè)一般區(qū)的周轉(zhuǎn)盤清洗間,再進入C級區(qū)精洗、滅菌。對應(yīng)B級區(qū)的清潔消毒,在C級區(qū)設(shè)置消毒液配制間,過濾后進入B級區(qū)精濾后使用。
2.3改造后無菌制劑車間布局
考慮到設(shè)備承重基礎(chǔ)及原有配套公用工程管道的要求,盡量減少重大改動,因此不改變凍干機原有的擺放位置。按《建筑設(shè)計防火規(guī)范》的要求,加設(shè)潔凈區(qū)的消防安全出口。據(jù)《建筑設(shè)計防火規(guī)范》的要求,加設(shè)潔凈區(qū)的消防安全出口。據(jù)上述幾個設(shè)計要點對原車間改造設(shè)計,改造后的無菌制劑車間設(shè)備平面布置圖見圖3。
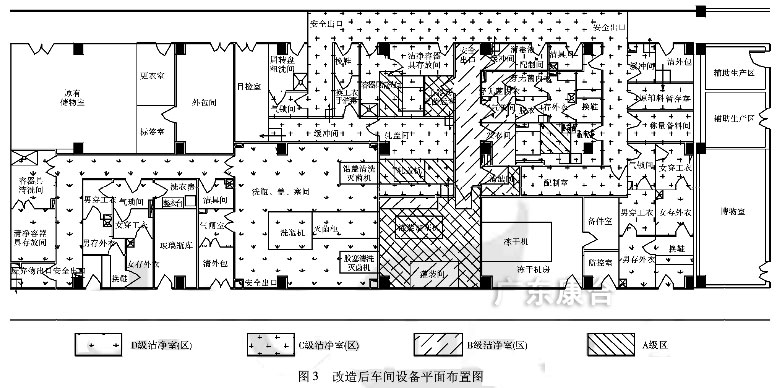
新版GMP規(guī)范作為質(zhì)量管理體系的一部分,是藥品生產(chǎn)管理和質(zhì)量控制的基本要求,旨在最大限度地降低藥品生產(chǎn)過程中污染、交叉污染以及混淆、差錯等風(fēng)險,確保持續(xù)穩(wěn)定地生產(chǎn)出符合預(yù)定用途和注冊要求的藥品。一個新規(guī)范的施行,必然帶來新的技術(shù)和新的觀念,對于設(shè)計人員須在實踐中不斷地進行探索與修正。本文僅從無菌制劑方面去進行分析,對新版藥品GMP中無菌藥品附錄的工藝生產(chǎn)要求進行討論,使設(shè)計能夠滿足新規(guī)范的要求。廣州化工2011年39卷第14期,作者:李穎君
無菌制劑車間改造; 藥品GMP無菌車間
- 1廣州黃埔區(qū)實驗室改造建設(shè)項目進行中
- 2公司參展2022年醫(yī)學(xué)實驗室建設(shè)展覽會簡報
- 3廣州黃埔區(qū)實驗臺通風(fēng)柜制造商圖片【廠家
- 4帶大家認識下第三方檢測實驗室
- 5PCR實驗室平面布局、通風(fēng)空調(diào)系統(tǒng)設(shè)計要點
- 6盤點:第三方醫(yī)學(xué)檢驗實驗室的優(yōu)勢和劣勢
- 7醫(yī)用潔凈室裝飾材料施工驗收規(guī)定
- 8中藥廠實驗室應(yīng)該配置哪些儀器設(shè)備?具體
- 9中藥飲片研發(fā)中心實驗室建設(shè),把握好這
- 10送你一份化學(xué)實驗室籌備方案




